化学上可以通过多种反应得到氨气[NH3],(氨气极易溶于水,相同条件下密度比空气小)
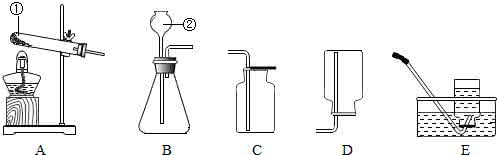
例如:
①2NH4Cl(固)+Ca(OH)2(固)△.
试题答案
分析:(1)据常用仪器回答;(2)制取较纯净的氨气,选择实验室制取NH3的反应原理;根据反应原理选择制取装置;根据“NH3(极易溶于水,密度比空气小)”,选择收集装置;归纳比较O2(或H2或CO2)的制取反应原理、制取与收集方法,书写相应的方程式;(3)总结归纳实验室制取O2、H2、CO2三种气体的反应原理、制取与收集方法;归纳出实验室制取气体反应的共同点和不同点.解答:解:(1)标号仪器分别是试管和长颈漏斗;(2)根据实验室制取NH3的反应原理,选择化学方程式为:①2NH4Cl(固)+Ca(OH)2(固)△.CaCl2+2NH3↑+2H2O或③CaO(固)+NH3?H2O(浓)=NH3↑+Ca(OH)2;根据反应物的状态和反应条件,若用方法①制取需要加热,属于固体加热型,选择发生装置A,若用方法③制取不需加热,属于固液常温型,选择发生装置B;根据“NH3(极易溶于水,密度比空气小)”,选择收集方法为:向下排空气法;若用方法①制取氨气,还可用来制取氧气,方程式是:2KMnO4△.K2MnO4+MnO2+O2↑;若用方法③制取氨气,还可用来制取O2(或H2或CO2),它们反应的化学方程式是:2H2O2MnO2.2H2O+O2↑或Zn+H2SO4=ZnSO4+H2↑或CaCO3+2HCl=CaCl2+CO2↑+H2O;(3)总结归纳实验室制取O2、H2、CO2三种气体的反应原理、制取与收集方法;归纳出实验室制取气体反应的共同点:③没有气体参加反应,⑤只生成一种气体;不一定需要加热,使用催化剂,如二氧化碳、氢气的制取,原料可能为混合物,如二氧化碳制取用大理石,故相同点为:③⑤;故答案为:(1)①试管;②长颈漏斗;(2)①(或③);A(或B);D;O2(或H2或CO2);2KMnO4△.K2MnO4+MnO2+O2↑(或2H2O2MnO2.2H2O+O2↑或Zn+H2SO4=ZnSO4+H2↑或CaCO3+2HCl=CaCl2+CO2↑+H2O);(3)③⑤.点评:总结归纳的方法是学习化学的重要方法;了解并掌握实验室制取氧气、氢气、二氧化碳的方法,并能根据相关知识分析解答问题,注重考查学生对知识的运用能力.
 爱华网
爱华网



