溴乙烷,无色油状液体,有类似乙醚的气味和灼烧味,露置空气或见光逐渐变为黄色,易挥发,能与乙醇、乙醚、氯仿和多数有机溶剂混溶。其蒸气有毒,浓度高时有麻醉作用,能刺激呼吸道。溴乙烷是通过溴化钾与冷冻的硫酸和乙醇反应而成。溴乙烷在水溶液中或熔化状态下均不电离,是非电解质。醇水积等略超酸,缓加震荡冷水冷。蒸馏,馏出液用3%碳酸钠溶液中和,静置2h分取有机相即为溴乙烷。原料消耗定额:乙醇(95%)557kg/t、氢溴酸(48%)1610kg/t、硫酸(92%)1165kg/t。
溴乙烷_溴乙烷 -基本内容
溴乙烷
Bromoethane
分子量108.9651
化学式:C2H5Br 缩写为EtBr。 结构简式:CH3-CH2Br
别名:乙基溴乙烷
CAS No.: 74-96-4
官能团:-Br
水中溶解度(g/100g):0℃时1.067,10℃时0.965,20℃时0.914,30℃时0.986。
相对密度(d20 4(20上标,4下标)1.4612。
凝固点-119℃。
沸点38.4℃。
折光率(n20 D(20上标,D下标))1.4242。
蒸气有毒。浓度高时有麻醉作用。能刺激呼吸道。溴乙烷在水溶液中或熔化状态下均不电离,是非电解质。
作用
是有机合成的重要原料。农业上用作仓储谷物、仓库及房舍等的熏蒸杀虫剂。溴乙烷是通过溴化钾与冷冻的硫酸和乙醇反应而成。常用于汽油的乙基化,冷冻剂和麻醉剂。因此,化工生产工人和熏蒸工都可接触不同浓度的溴乙烷。
在有机合成中,EtBr是假想乙基碳正离子(Et)的合成子。例如可将由羧酸盐转化为乙酯,碳负离子至乙基衍生物,硫脲至乙基异硫脲盐, 及胺至乙基胺。即使此液体存在于室温,仍然很易挥发。EtBr常用作制备强碱性的格林尼亚试剂,如EtMgBr可使炔失去质子:EtBr + Mg → EtMgBr
RC≡CH + EtMgBr → RC≡CMgBr +EtH此应用已被有机锂试剂广泛取代。
贮存
切记密封避光保存。
化学性质
水解反应
C2H5Br+NaOH→C2H5OH+NaBr(氢氧化钠水溶液共热)
消去反应
溴乙烷
CH3CH2Br+NaOH→C2H4+NaBr+H2O(氢氧化钠乙醇共热)
溴乙烷_溴乙烷 -制法
工业制法
NaBr + H3PO4 === NaH2PO4 + HBr
CH3CH2OH + HBr→H2O + CH3CH2Br
CH2CH2+HBr→CH3CH2Br
实验室制法
NaBr+H2SO4==HBr+NaHSO4 ①
R-OH+HBr==R-Br+H2O ②
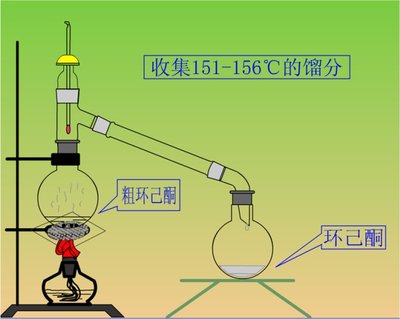
将乙醇溶于一定量的水中,倒入烧瓶待用。稀释浓硫酸,待冷却至室温后并加入NaBr搅拌均匀,加入盛有乙醇的烧瓶中。连接分馏装置,冷却装置,接收瓶中倒入冰水混合物。实验过程中若混合物剧烈沸腾需降低温度。在接收瓶中沉于底部的油状物质即为C2H5Br
溴乙烷_溴乙烷 -相关口诀
醇水积等略超酸,缓加震荡冷水冷。需加碎瓷防暴沸,隔网小火方可行。
除醇用水冰浴冷,溴烷无色常橘红。除溴需用碱液洗,漏斗分液便告成。
解释:
(1)醇水积等略超酸:“醇”在此指乙醇,“酸”在此指浓硫酸,“积等”在此指乙醇与水的体积相等,这句的意思是说,实验所用的乙醇与水的体积相等,而且要求乙醇与水的体积之和略超过浓硫酸的体积(在该实验中要求所用硫酸不能太稀也不能太浓,因为反应原理为:NaBr+H2SO4=NaHSO4+HBr,C2H5OH+HBr→C2H5Br+H2O。如果硫酸太浓,则第一步生成的HBr还没来得及和乙醇反应就被H2SO4氧化成单质的溴了:2HBr+H2SO4=SO2↑+2H2O+Br2;若硫酸太稀则反应速度太慢。实践证明,乙醇与水的体积相等,而且乙醇与水的体积之和略超过浓硫酸的体积的情况下,反应效果较理想,因而课本中乙醇与水的体积各为8ml,浓硫酸为15ml)。
(2)缓加震荡冷水冷:意思是说浓硫酸要缓缓加入盛乙醇溶液的烧杯中,同时不断震荡烧杯,并用冷水冷却至室温(否则会因浓硫酸稀释时产生的大量的热造成温度过高而导致乙醇蒸发)。
(3)隔网小火方可行:意思是说加热烧瓶时务必要隔着石棉网用小火加热(如果直接加热,则因温度太高,大量乙醇还没有来得及与HBr反应就蒸发了)。
(4)除醇用水冰浴冷:“除醇用水”的意思是说在U型管中需加少量的蒸馏水,其作用是除去随溴乙烷蒸发出来的少量乙醇,因为乙醇极易溶解入水;“冰浴冷”的意思是说收集溴乙烷的U型管务必放在冰水中冷却,因为溴乙烷的沸点较低易挥发。
(5)溴烷无色常橘红:“溴烷”指溴乙烷。这句的意思是说溴乙烷本为无色油状液体,但制得的溴乙烷通常是橘红色,这是因为硫酸把生成的HBr部分氧化为溴而溶于溴乙烷中了。
(6)除溴需用碱液洗,漏斗分液便告成:这句的意思是说,除掉溴乙烷中的溴,可用碱液(常用10%的NaOH)洗涤后,再用分液漏斗分离即可
。
溴乙烷_溴乙烷 -侵入途径
接触者以呼吸道吸入为主。液体也可经污染的皮肤吸收。
溴乙烷_溴乙烷 -毒理学简介
大鼠经口LD50: 1350 mg/kg; 吸入LC50: 26980 ppm/1H。小鼠吸入LC50: 16230 ppm/1H。
毒作用与溴甲烷相似,但毒性较小,具有麻醉作用,可引起肺部刺激和肝、肾、心脏的损害。动物实验证明,吸入高浓度溴乙烷后,可产生中枢麻痹、呼吸抑制而死亡。
无论对人或动物都可引起严重的神经系统和呼吸系统损害。
对人的麻醉浓度为1.34~4.46g/m3
溴乙烷_溴乙烷 -临床表现
急性中毒后出现以中枢神经系统和呼吸系统为主的症状,特征是面部潮红、瞳孔扩大、脉搏加快以及头痛、眩晕等症状。严重者有四肢震颤、呼吸困难、发绀、虚脱,甚至呼吸麻痹。
根据密切接触史,短时间内出现的以神经系统和呼吸系统损害为主的临床表现,参考现场卫生学调查,排除类似表现的疾病,综合分析后,诊断是不困难的。
溴乙烷_溴乙烷 -处理
中毒患者应立即脱离现场。脱去污染的衣着,污染的皮肤用大量清水冲洗。
以支持治疗为主,并给予对症治疗。无特效解毒剂。
溴乙烷_溴乙烷 -安全
卤代烃通常是带有潜在危险的烷基化剂,溴化物较氯化物烷基化能力更强,因此应尽量避免接触EtBr。EtBr被美国加州列入致癌物质及一种生殖上的毒素。
溴乙烷_溴乙烷 -物质毒性
文献、期刊报道的毒性作用试验数据编号毒性类型测试方法测试对象使用剂量毒性作用1急性毒性口服大鼠1350 mg/kg详细作用没有报告除致死剂量以外的其他值2急性毒性吸入大鼠26980 ppm/1H详细作用没有报告除致死剂量以外的其他值3急性毒性腹腔注射大鼠1750 mg/kg详细作用没有报告除致死剂量以外的其他值4急性毒性吸入小鼠16230 ppm/1H1.行为毒性――嗜睡2.胃肠道毒性――运动过度、腹泻5急性毒性腹腔注射小鼠2850 mg/kg详细作用没有报告除致死剂量以外的其他值6慢性毒性吸入大鼠2 pph/6H/14D-I1.慢性病相关毒性――死亡7慢性毒性吸入大鼠1600 ppm/6H/14W-I1.血液毒性――脾发生变化
2.慢性病相关毒性――死亡8慢性毒性吸入小鼠1 pph/6H/14D-I1.慢性病相关毒性――死亡9突变毒性
鼠伤寒沙门氏菌75 ng/plate
10突变毒性
仓鼠卵巢100 mg/L
11致癌性吸入大鼠100 ppm/6H/2Y-I1.致癌性――可能致癌(根据RTECS标准)
2.大脑毒性――肿瘤12致癌性吸入小鼠200 ppm/6H/2Y-I1.致癌性――致癌(根据RTECS标准)
2.生殖毒性――子宫肿瘤
溴乙烷_溴乙烷 -物性数据
1.性状:无色易挥发液体
2.熔点(℃):-119
3.沸点(℃):38.4
4.相对密度(水=1):1.45(25℃)
5.相对蒸气密度(空气=1):3.76
6.饱和蒸气压(kPa):53.2(20℃)
7.燃烧热(kJ/mol):-1423.3
8.临界温度(℃):776.8
9.临界压力(MPa):6.23
10.辛醇/水分配系数:1.61
11.闪点(℃):-23
12.引燃温度(℃):511
13.爆炸上限(%):11.3
14.爆炸下限(%):6.7
15.溶解性:不溶于水,溶于乙醇、乙醚等多数有机溶剂。
16.临界密度(g・cm-3):0.507
17.临界体积(cm3・mol-1):215
18.临界压缩因子:0.320
19.偏心因子:0.183
20.溶度参数(J・cm-3)0.5:18.475
21.van der Waals面积(cm2・mol-1):5.550×109
22.van der Waals体积(cm3・mol-1):38.300
23.液相标准声称热(焓)( kJ・mol-1):-91.8
24.液相标准热熔(J・mol-1・K-1):100.5
25.气相标准声称热(焓)( kJ・mol-1) :-63.6
26.气相标准熵(J・mol-1・K-1) :287.36
27.气相标准生成自由能( kJ・mol-1):-25.7
28.气相标准热熔(J・mol-1・K-1):64.23
溴乙烷_溴乙烷 -存储方法
储存注意事项 储存于阴凉、通风的库房。远离火种、热源。保持容器密封。应与氧化剂、碱类、食用化学品分开存放,切忌混储。采用防爆型照明、通风设施。禁止使用易产生火花的机械设备和工具。储区应备有合适的材料收容泄漏物。
溴乙烷_溴乙烷 -合成方法
1.由乙醇与溴化钠反应而得:在反应锅内加入40%溴化钠溶液及乙醇,搅拌下加入硫酸,温度不超过50℃。加完后在45-50℃反应2h。蒸馏,馏出液用3%碳酸钠溶液中和,静置2h分取有机相即为溴乙烷。原料消耗定额:乙醇(95%)557kg/t、氢溴酸(48%)1610kg/t、硫酸(92%)1165kg/t。
2.由乙醇和溴素反应而得:搅拌下将溴素慢慢加到硫黄和水的悬浮液中,温度保持在35-40℃。然后加入乙醇。在25-28℃加入硫酸,反应42h。蒸馏,收集38-39℃馏分即得溴乙烷。收率90%左右。原料消耗定额:乙醇770kg/t、溴素250kg/t、硫酸1042kg/t、硫磺18kg/t。方法(1)中,也可以用氢溴酸与乙醇反应,制备过程与溴化钠法相同,收率都为96%,另外由乙烯与溴化氢加成或由乙烷溴化都可以得到溴乙烷。工业品溴乙烷纯度≥98%。
3.以工业品溴乙烷为原料,用浓硫酸洗涤数次,用水洗涤一次,再用10%的碳酸钠溶液洗涤2次,用5%的硫代硫酸钠溶液洗涤一次,静置分去水层,用无水氯化钙干燥后,精馏,收集37~40℃馏分即为成品。
4.制法:
于装有搅拌器、滴液漏斗、蒸馏装置的反应瓶中,加入48%的氢溴酸41.5g(2.81mol),水浴冷却,搅拌下慢慢加入浓硫酸120g(65mL),再加入95%的乙醇(2)100g(2.06mol),慢慢加热,并由滴液漏斗滴加浓硫酸109mL,同时蒸出生成的溴乙烷。接引管伸入接受瓶中水面下,接受瓶用冰水冷却。待无溴乙烷蒸出时,停止反应。分出馏出物种的粗溴乙烷,依次用水、5%的碳酸钠溶液、水洗涤,无水氯化钙干燥。水浴加热蒸馏,收集38~39℃的馏分,得溴乙烷(1)205g,收率91%。
5.制法:
于反应瓶中加入95%的乙醇(2)100mL(1.7mol),水90mL,不断搅拌下慢慢加入浓硫酸190mL,反应放热,注意冷却至室温。搅拌下慢慢加入研细的溴化钠163g(1.5mL),和几粒沸石。安上蒸馏装置,接受瓶中加入适量冰水,并将其置于冰浴中。慢慢加热,使反应和蒸馏平稳进行,直至无油状物镏出为止。分出有机层,硫酸干燥。蒸馏,收集35~40℃的馏分,得溴乙烷(1)100~120g,收率61%~74%。
溴乙烷_溴乙烷 -主要用途
1.是有机合成的重要原料。农业上用作仓储谷物、仓库及房舍等的熏蒸杀虫剂。溴乙烷是通过溴化钾与冷冻的硫酸和乙醇反应而成。常用于汽油的乙基化,冷冻剂和麻醉剂。因此,化工生产工人和熏蒸工都可接触不同浓度的溴乙烷。2.溴乙烷是制造巴比妥的原料。还用作制冷剂、麻醉剂、溶剂、熏蒸剂、有机合成等方面。3.用作分析试剂,如作溶剂、折射率标准样品。还用于有机合成及航空工业用灭火剂。4.用于有机合成,用作溶剂、制冷剂,也用于医药工业。
溴乙烷_溴乙烷 -安全信息
风险术语
R11:Highly flammable. 高度易燃。
R20/22:armful by inhalation and if swallowed. 吸入及吞食有害。
R40:Limited evidence of a carcinogenic effect. 少数报道有致癌后果。
安全术语
S36/37:Wear suitable protective clothing and gloves.穿戴适当的防护服和手套。
溴乙烷_溴乙烷 -系统编号
CAS号:74-96-4
MDL号:MFCD00000232
EINECS号:200-825-8
RTECS号:KH6475000
BRN号:1209224
PubChem号:24854383
溴乙烷_溴乙烷 -毒理学数据
1.急性毒性
LD50:1350mg/kg(大鼠经口)
LC50:72386mg/m3(小鼠吸入,1h)
2.刺激性 暂无资料
分子结构
1、摩尔折射率:19.04
2、摩尔体积(m3/mol):74.7
3、等张比容(90.2K):163.8
4、表面张力(dyne/cm):23.1
5、介电常数:
6、偶极距(10-24cm3):
7、极化率:7.55
溴乙烷_溴乙烷 -计算化学
1、疏水参数计算参考值(XlogP):1.4
2、氢键供体数量:0
3、氢键受体数量:0
4、可旋转化学键数量:0
5、拓扑分子极性表面积(TPSA):0
6、重原子数量:3
7、表面电荷:0
8、复杂度:2.8
9、同位素原子数量:0
10、确定原子立构中心数量:0
11、不确定原子立构中心数量:0
12、确定化学键立构中心数量:0
13、不确定化学键立构中心数量:0
14、共价键单元数量:1
溴乙烷_溴乙烷 -生态学数据
1.生态毒性 暂无资料
2.生物降解性 MITI-I测试,初始浓度100ppm,污泥浓度30ppm,4周后降解13%~45%。
3.非生物降解性 空气中,当羟基自由基浓度为5.00×105个/cm3时,降解半衰期为46d(理论)。在25℃,当pH值为7时,水解半衰期为30d(理论)。
4.其他有害作用 该物质对环境有危害,应特别注意对水体的污染。
溴乙烷_溴乙烷 -性质稳定性
1.溴乙烷是有甜味的可燃性液体,在光照或火焰下易分解生成溴化氢和碳酰溴,后者有类似光气的剧毒作用。
2.与强碱的醇溶液反应生成乙烯,在强碱的水溶液中水解生成乙醇。
3.稳定性 稳定
4.禁配物 强碱、强氧化剂、镁
5.避免接触的条件 受热、光照
6.聚合危害 不聚合
7.分解产物 溴化氢
 爱华网
爱华网