相关解答一:氧化和氧化剂如何判断
化剂得电子,发生氧化反应。
某离子氧化化合价是上升,被氧化,化合价降低,生成氧化产物,被还原,生成还原产物,化合价升高,发生还原反应。
还原剂失电子。
氧化=被氧化
相关解答二:如何判断氧化剂和还原剂 口诀 5分
升(化合价)失(电子)氧(氧化物 氧化反应) 降(化合价)得(电子)还(还原物 还原反应) 若说剂 正相反
相关解答三:如何判断一个物质是作氧化剂还是还原剂?~~~~
水嘛,一般来说物质是不太和水反应滴,但如果题目出来了,应该就是做氧化剂(如果是复分解就不是了),也有例外的,不知道你说的是什么情况
氧化剂和还原剂跟物质里有几种元素是没有关系滴,就比如氧化铜和氢气反应生成铜和水,把氧元素撇开不管,铜的化合价由2降低为0,就称为被还原,氧化铜就是氧化剂(氧气或含氧化合物);氢的化合升高,就是被氧化,氢气就是还原剂。。。懂了哇
相关解答四:如何判断一个物质是氧化剂还是还原剂
因此某种物质究竟是氧化剂还是还剂一个物质是氧化剂还是还原剂!
在具体的反应中,那么在反应中就是氧化剂。那它就是还原剂,要视“对手”而言。反之它就是氧化剂,经过反应,若其化合价升高了,没有绝对而明确的界定!当某物质遇到氧化性比它强的,那么在反应中它就是还原剂,若是遇到氧化性比它弱的
相关解答五:如何判断一种物质是否为氧化剂?要初中生看得懂 30分
氧化还原反应中,化合价升高的物质,化合价降低的物质,是氧化剂,是还原剂,被还原,被氧化
相关解答六:如何判断氧化剂和还原剂,他们的含义又是什么?谢谢你们的回答!
一个化学反应完成后,最后得到电子的是氧化剂,失去电子的是还原剂。
氧化剂是氧化还原反应里得到电子或有电子对偏向的物质。氧化剂从还原剂处得到电子自身被还原变成还原产物。
还原剂是在氧化还原反应里,失去电子或有电子对偏离的物质。
跟你怎么说你可能不明白,看看下面的东西,可能对你有所帮助:
—氧化还原反应是在反应前后,某种元素的化合价有变化的化学反应。这种反应可以理解成由两个半反应构成,即氧化反应和还原反应。
复分解反应都不是氧化还原反应
置换反应都是氧化还原反应
有单质参加的化合反应大部分是氧化还原反应(有例外)
有单质生成的分解反应大部分是氧化还原反应(例外如次氟酸分解:2HFO==2HF+O2,化合价没有变化)
归中反应,岐化反应可以看作是特殊的氧化还原反应
另外要注意,有单质参加反应的化学反应不一定是氧化还原反应,如氧气生成臭氧
概念
反应的本质是化合价有变化,即电子有转移。氧化数升高,即失电子的半反应是氧化反应;氧化数降低,得电子的反应是还原反应。化合价升高的物质还原对方,自身被氧化,因此叫还原剂,其产物叫氧化产物;化合价降低的物质氧化对方,自身被还原,因此叫氧化剂,其产物叫还原产物。即:
还原剂 + 氧化剂 ---> 氧化产物 + 还原产物
一般来说,同一反应中还原产物的还原性比还原剂弱,氧化产物的氧化性比氧化剂弱,这就是所谓“强还原剂制弱还原剂,强氧化剂制弱氧化剂”。
凡例
氢气与氯气的化合反应
氢气与氯气的化合反应,其总反应式如下:
H2 + Cl2 → 2HCl
我们可以把它写成两个半反应的形式:
氧化反应:
H2 → 2H+ + 2e-
还原反应:
Cl2 + 2e- → 2Cl-
单质总为0价。第1个半反应中,氢元素从0价被氧化到+1价;同时,在第2个半反应中,氯元素从0价被还原到−1价. (本段中,“价”指氧化数)
两个半反应加合,电子数削掉:
H2 → 2H+ + 2e-
+ 2e- + Cl2 → 2Cl-
---------------------
H2 + Cl2 → 2H+ + 2Cl-
最后,离子结合,形成氯化氢:
2H+ + 2Cl- → 2HCl
————
配平碳与硝酸起反应的化学方程式
解∶1,写出反应物和生成物的化学式
C+HNO3→NO2+CO2+H2O
2,列出元素的化合价的变化
在反应物这边 在生成物这边 变化量
C化合价 0 +4 升高4
N化合价 +5 +4 降低1
3,使化合价的升高和降低的总数相等
C+4HNO3→4NO2+CO2+H2O
4,配平其它物质的系数
C+4HNO3═4NO2↑+CO2↑+2H2O
————
与电化学的关系
每一个氧化还原反应都可以做成一个原电池。其中发生氧化反应的一极为阳极,即外电路的负极;还原反应的一极为阴极,即外电路的正极。两个电极之间有电势差(电化学上通常叫电动势),因此反应可以进行,同时可以用来做功。
名称来源
氧化反应最早是指金属或非金属与氧结合形成氧化物的反应,这类反应中另一种元素的化合价总是升高。还原反应最早是指金属从其化合物中被提炼出来的反应,这类反应中金属的化合价......余下全文>>
相关解答七:怎样根据离子方程式判断出氧化剂和还原剂
一.同一元素形成的不同物质的氧化性,还原性强弱的判断方法。 (一)根据元素化合价判断。最高价只有氧化性,最低价只有还原性,中间价既有氧化性又有还原性。与S元素+6价时只有氧化性(浓硫酸),-2价时只有还原性,+4价既有氧化性又有还原性(SO2)。 (二)根据物质的浓度大小判断 。具有氧化性(或还原性)的物质浓度越大,其氧化性(或还原性)越强,反之则越弱。如浓H2SO4的氧化性>稀H2SO4,浓HNO3的氧化性>稀HNO3 二。不同物质或不同元素的氧化性,还原性强弱的判断方法 (一)根据化学方程式判断 (1)氧化剂(氧化性)+还原剂(还原性)===还原产物+氧化产物 氧化性:氧化剂>氧化产物 还原性:还原剂>还原产物 (2)可根据同一个反应中的氧化剂,还原剂判断 氧化性:氧化剂>还原剂 还原性:还原剂>氧化剂 (二)根据反应条件判断,当不同氧化剂分别于同一还原剂反应时,如果氧化产物价态相同,可根据反应条件的难易来判断。反应越容易,该氧化剂氧化性就强。 如:16HCl(浓)+2KMnO4==2KCl+2MnCl2+8H2O+5Cl2(气) 4HCl(浓)+MnO2===(加热)MnCl2+2H2O+Cl2(气) 4HCl(浓)+O2==(加热,CuCl2催化剂)2H2O+2Cl2(气) 氧化性:KMnO4>MnO2>O2 (三)根据氧化产物的价态高低来判断 当含有变价元素的还原剂在相似的条件下作用于不同的氧化剂时,可根据氧化产物价态的高低来判断氧化剂氧化性强弱。如: 2Fe+3Cl2==(点燃)2FeCl3 Fe+S==(加热)FeS 氧化性:Cl2>S (四)根据物质活动性顺序比较 (1)对于金属还原剂来说,金属单质的还原性强弱一般与金属活动性顺序一致。 还原性:K>Ca>Na>Mg>Al>Mn>Zn>Cr>Fe>Ni>Sn>Pb>(H)>Cu>Ag>Pt>Au (2)金属阳离子氧化性的顺序 一般与金属活动性顺序相反。 K+
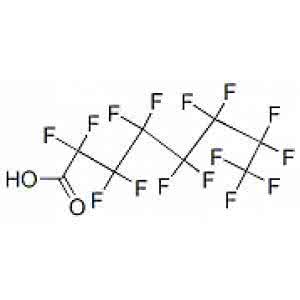
相关解答八:如图,如何判断这个化合物为手性分子。
我们知道,生命是由碳元素组成的,碳原子在形成有机分子的时候,4个原子或基团可以通过4根共价键形成三维的空间结构.由于相连的原子或基团不同,它会形成两种分子结构.这两种分子拥有完全一样的物理、化学性质.比如它们的沸点一样,溶解度和光谱也一样.但是从分子的组成形状来看,它们依然是两种分子.这种情形像是镜子里和镜子外的物体那样,看上去互为对应.由于是三维结构,它们不管怎样旋转都不会重合,就像我们的左手和右手那样,所以又叫手性分子.
对于非碳原子手性中心的分子,只要没有对称面和对称中心即为手性分子.
手性分子的基本标志
一个化合物的分子与其镜像不能互相叠合,则必然存在一个与镜像相应的化合物,这两个化合物之间的关系,相当于左手和右手的关系,即互相对映.这种互相对应的两个化合物成为对映异构体(enantiomers).这类化合物分子成为手性分子(chiral molecule).不具有对称面和对称中心的分子有一个重要的特点,就是实体和镜象不能重叠,镜面不对称性是识别手性分子与非手性分子的基本标志.
生物分子手性原则是什么
生物分子都有手性,即分子形式的右撇子和左撇子(或左旋、右旋).在法国生物学家巴斯德发现酒石酸晶体的镜像后就更激起了科学家的兴趣.然而,手性分子是如何形成的却一直让人迷惑不解.过去,生物化学领域趋向于认为,单一手性形式的分子合成通常从一开始就要利用手性本体,也就是说生物分子自身在催化着手性形式的形成.而且在一些化学反应中手性产物的形成进一步扩大了.
相关解答九:怎么判断一个化合物熔沸点高低?
1,首先要确定化合物种类。只有同种化合物种类才能以微观的角度去判断熔点或沸点。
2,针对离子化合物,他含有离子键的强度是决定熔点的主要因素,离子键的键能越高,则所需要的能量也越高,所以熔点也就高。
3,离子键强度取决与离子的半径以及所带电荷量。通常半径大,熔点小。电荷量大,熔点高。
费点
有机化和物的沸点高低有一定的规律,现总结如下:
1、同系物沸点大小判断,一般随着碳原子数增多,沸点增大。
如甲烷<乙烷<丙烷<丁烷<戊烷<.....
2、链烃同分异构体沸点大小判断,一般支链越多,沸点越小。
如:正戊烷>异戊烷>新戊烷
3、芳香烃的沸点大小判断,侧链相同时,临位>间位>对位。
如:临二甲苯》间二甲苯》对二甲苯
4、对于碳原子数相等的烃沸点大小判断,烯烃<烷烃<炔烃
5、同碳原子的脂肪烃的衍生物沸点大小判断,烯烃的衍生物沸点低于烷烃的同类衍生物。
如:油酸的沸点<硬脂酸
6、不同类型的烃的含氧衍生物的沸点比较,相对分子质量相近的脂肪羧酸>脂肪醇>
脂肪醛
7、酚和羧酸与它们对应的盐沸点比较,酚和羧酸<对应盐的沸点。如乙酸<乙酸钠
8、分子量相近的烃的沸点一般低于烃的衍生物。
相关解答十:如何判断化合物是否具有氧化性?
化合物具有氧化性,经过化学反应后被还原化合价降低,只要看某元素的化合价在化学反应前后有没有降低就行了
百度搜索“爱华网”,专业资料,生活学习,尽在爱华网
 爱华网
爱华网