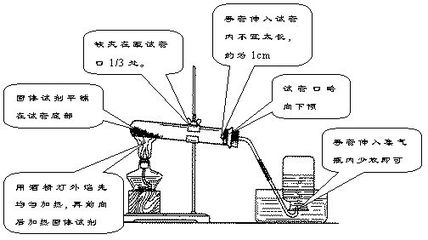
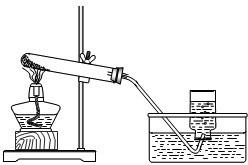
2.2-3 氯酸钾制取氧气(1)
要得到O2,应当到富含这种物质的 地方去寻找,哪些物质是富含氧元 素的呢?
含有氧气的混合物或者含氧化合物
空气中主要含有氧气和氮气,为了得到较为 纯净的O2,如何将N2和O2分离呢?
N2 溶解性 沸点 熔点 密度 难 -195.8℃ -209.86℃ 比空气略小
O2 难 -183.0℃ -218.4℃ 比空气略大
请利用以上不同物理性质,设计实验将 N2和O2分离?
一、分离液态空气(物理变化) 空气
净化、加压降温
液态空气 升温
N2汽化 剩下的主要是液态氧 (混合物) 注:利用沸点不同
1、分离液态空气方法利用的是O2和N2的什么物理 性质不同? 2、该方法是物理变化还是化学变化? 3、得到的液氧是纯净物还是混合物?
巩固练习
沸点 不 1、分离液态空气方法是利用O2和N2的________ 物理 变化(填“物理” 同进行分离,该方法是________ 混合物 或 “化学”),得到的液氧是 __________(填“纯 净物”或“混合物”)
2、空气中的主要成分是氮气和氧气。液氮的沸 点是-196℃,液氧的沸点是-183℃.现打开一只装有 液态空气的容器盖,并将一根燃着的木条置于容器 口上方,观察到的现象是( B ) A、燃烧得更旺 B、燃着的木条火焰熄灭 C、无明显变化 D、燃烧得更旺后熄灭
除了选择分离液态 空气这种物理方法制氧 气以外,还可以通过化学方法制取氧气
如可以用氯酸钾和二氧化锰混合加热制氧气 (KClO3) (MnO2)
这两种物质都含有氧元素,那么氧气是哪 种物质产生的呢?
演示实验
步骤:
分别加热KClO3和MnO2,并用带火星 的木条检验是否产生O2,观察实验现象
结论:
加热KClO3熔化并沸腾时能有少量 O2放 出,MnO2加热条件下不能放出 O2
反思:
那么MnO2在氯酸钾和二氧化锰混合加 热制氧气的反应中起什么作用?
演示实验
步骤:
加热KClO3至熔化,然后向试管中加入 一定量的MnO2,并用带火星的木条检 验,观察实验现象
结论:
MnO2能加快KClO3放出O2的速率
二、氯酸钾制氧气 1、反应原理
氯酸钾
KClO3
二氧化锰 加热
氯化钾 + 氧气
KCl O2
2、催化剂:能加快反应速率,但本身的 质量 化学性质 质量和化学性质在反应前后没有变化 (一变两不变) 二氧化锰是氯酸钾制取氧气反应的催化剂 MnO2能加快KClO3放出O2的速率,但 单凭这点能说明MnO2是KClO3分解的 催化剂吗?
氯酸钾
二氧化锰 加热
氯化钾 + 氧气
请设计实验证明它的质量和化学性质在 反应前后是否有改变?
巩固练习
3、氯酸钾和二氧化锰的混合物加热制取氧气 时,二氧化锰的作用是( D) A、加快反应速率,增加氧气的产量 B、增加氧气的产量 C、不加二氧化锰,加热氯酸钾不能产生氧气 D、
加快反应速率,但是不增加氧气的产量
4、(1)在加热氯酸钾和二氧化锰混合物的 催化剂 ,反应前后它的 反应中,二氧化锰是_______ 化学性质 都没有改变,它的作用是 质量 和__________ _____ 加快反应速率 。 ________________ (2)氯酸钾和二氧化锰的混合物制取氧气 二氧化锰 氯酸钾 氯化钾 + 氧气 的文字表达式是 _________________________ 。 加热 充分反应后的残留固体和足量的水混合,经 二氧化锰 , 搅拌、过滤,所得黑色滤渣是___________ 氯化钾 滤液中的溶质是______________ 。
氯酸钾和二氧化锰的混合物加热制取氧 气的反应是化合反应吗? 如果不是,它的反应类型是什么?
氯酸钾 二氧化锰 氯化钾 + 氧气
加热
3、分解反应 由一种物质生成两种或两种以上新物 质的反应(一分多)
工业上常需要制得大量的氧气,而实验室研 究时则需要少量但较纯的氧气,今天我们学 习的两种方法都能得到氧气,哪种适合工业 制氧气?哪种适合实验室制氧气? 氧气制法: 工业:1、分离液态空气
2、电解水 实验室: 1、加热氯酸钾和二氧化锰混合物 2、加热高锰酸钾(KMnO4)
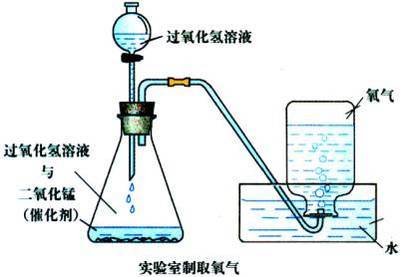
3、过氧化氢和二氧化锰混合
巩固练习 B ) 5、工业上制取大量氧气的方法是( A、加热高锰酸钾 B、分离液态空气 C、电解水 D、加热氯酸钾
6、下列说法正确的是( D ) A、氯酸钾中含有氧气,加热时即可放出 B、从空气中可以得到氮气和氧气,这个变化 是分解反应 C、凡是含氧的物质都可以作为实验室制氧气 的原料 D、实验室用氯酸钾制氧气时发生了化学反应
7、要得到大量的气体,可以用工业制法;要得 到少量的气体,可以用实验室制取气体的方法。 选择实验室制取气体的原料一般规律是( D ) ①必须含有相关成分 ②易于反应常温更好 ③无毒无害没有污染 ④必须要用物理方法 ⑤节约能源价格便宜 ⑥装置简便易于操作 A、①③④⑤⑥ B、②③④⑤⑥ C、①②③④⑤ D、①②③⑤⑥
课堂练习
1、工业制取氧气所用的原料是空气,所发生的反 B ) 应是( A、化学变化 B、物理变化 C、化学变化和物理变化 D、无法确定 2、实验室用氯酸钾和二氧化锰的混合物加热制取 氧气时,对于二氧化锰来说发生改变的是( B ) A、反应前后的质量 B、反应前后在固体混合物中的质量分数 C、反应前后元素的化合价 D、反应前后的化学性质
3、同时加热下列物质,最易放出氧气的 一组物质是( D ) A、纯净的氯酸钾 B、混有二氧化锰的氯化钾 C、纯净的二氧化锰 D、混有二氧化锰的氯酸钾
4、研究表明,许多金属氧化物对氯酸钾的分解 有催【http://www.niubb.net/】化作用,下表是不同金属氧化物作催化剂 时氯酸钾剧烈反应的
 爱华网
爱华网