2009年5月23日下午,集美轻工业学校化学专业化学分析中级工滴定技能考试结束了,看着同学们忧愁无奈的表情,我就知道考试结果又不理想了。是什么考试题目让同学们这样紧张忧心呢?肯定是它——硫酸含量测定。这个题目前年考过,去年考过,今年又考到,这就说明硫酸含量测定这个考试内容既很重要又有难度,也笼罩了一层神秘的面纱。不是吗?不然这几年怎会年年考到呢?那么,这个普通的硫酸含量测定有何特别之处让同学们是那样的紧张甚至惧怕呢?它的神秘之处又在哪?
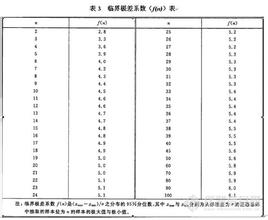
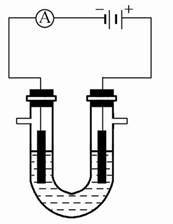
经过这几年的滴定技能实训、技能鉴定的观察、分析、探讨,我们不难发现所谓的神秘之处其实并不神秘,只不过是测定结果偏差较大而已。当然,千万不要小看这个测定结果,它可是不那么容易让你驯服的。在平时的实训及鉴定考试中它可是让同学们吃尽了苦头的。因为这个测定结果关系到滴定技能鉴定是否合格的最关键的条件。滴定技能鉴定考试规定,学生必须平行测定二份样品的结果,且而二份平行测定结果的极差不能超过0.4。这是什么概念呢?其实这就是测定结果的精确度(极差)问题。必须明确,滴定技能鉴定考试能否合格,关键就是看测定结果的准确度和精确度是否达标。我们知道,准确度(Accuracy)是指你得到的测定结果与真实值之间的接近程度。精确度(Precision)是指使用同种备用样品进行重复测定所得到的结果之间的重现性。测量的准确度高,是指系统误差较小,这时测量数据的平均值偏离真值较少,但数据分散的情况,即偶然误差的大小不明确。 测量精确度高,是指偶然误差与系统误差都比较小,这时测量数据比较集中在真值附近。本文探讨的是平行测定结果极差(精确度)问题。用硫酸含量测定这个例子来说明,有个同学的测定结果有一份含量是97.65%,另一份含量是97.13%,那么平行测定结果的极差就是0.52,超过0.4,属于不合格的结果。所以滴定结果极差对滴定技能鉴定能否合格影响极大,在滴定结果准确度达标的情况下,滴定结果极差(精确度)就成为能否合格的关键。前面我们提过,同学们对这个测定题目很害怕,因为这个滴定的平行测定结果的极差较难控制,稍不注意就达不到要求。真的有那么难那么神秘吗?下面我们就一步一步地来分析,共同探讨其中的奥妙。 首先,我们来说说硫酸(H2SO4)含量滴定的原理。硫酸是一种强酸,要测定它就得寻找一种既稳定易得又成本较低的强碱,配成容易标定的标准液,再通过普通的酸碱滴定来测定硫酸的含量。根据要求我们选定氢氧化钠(NaOH)作伪标准液来滴定硫酸从而算出硫酸的含量。其反应方程式如下: H2SO4+2NaOH==Na SO4+2H2O 滴定终点指示剂选用0.2%甲基红,其变色范围是pH404~6.2,溶液颜色由红色变为亮黄色时就是滴定终点。 所用试剂及仪器: 0.1mol/L NaOH标准液;H2SO4试样;0.2%甲基红指示剂 分析天平或电子天平 ;50ml碱式滴定管;250ml锥形瓶; 300ml、500ml烧杯各一个;玻棒;小滴管;洗瓶 操作过程及步骤:先确定硫酸试样的称取量,也就是要用密度计测出硫酸的密度,再用工具书查出本硫酸试样的大致百分含量,从而算出硫酸试样的称取量。一般来说,浓度在80%以上的可准确称取0.1~0.2克/份;浓度在40%-~80%的可称取0.2~0.4克/份。称取时试样装于胶帽滴瓶以便称取。称取量确定后,就要准确称取一定量的试样(准确称至0.0001克)放入已装有25ml蒸馏水的锥形瓶中,轻轻摇匀并使之冷却至室温,加入2滴0.2%甲基红指示剂,用0.1ml/NaOH标准液滴定至溶液颜色由红色变至橙色至暗黄色到亮黄色为终点,读取读数并做记录。平行测定2~3次,然后计算测定结果。计算公式如下: H2SO4%= c(NaOH)×V(NaOH) ×4.904/m(试样) 式中: C(NaOH)—-NaOH标准液的摩尔浓度,mol/L V(NaOH)---滴定终点NaOH标准液的用量,ml 4.904----1/2 H2SO4的摩尔质量(98.07)×100/1000的结果,g/mol m(试样)--- H2SO4试样的质量,g 通过操作步骤我们不难发现,这个滴定其实简单明了并不复杂,那么同学们为什么会做不出合格的平行测定结果的极差呢?问题出在哪里?经过不断的试验、探索、分析,我们认为有以下几个主要原因: .滴定终点不一致,也就是说有一份测定还未滴到终点,另一份却滴过量,这样滴定结果的极差肯定不合格。主要表现在终点判断不准确,即终点指示剂的颜色不一致。我们知道,指示剂甲基红的变色范围在Ph4.4~6.2之间,颜色变化是由红色→橙色→暗黄色→亮黄色。而由暗黄色到亮黄色只需1/2~1/4滴的滴液加入即可到达终点,过量的滴加滴液,终点颜色并不会改变依然还是亮黄色,所以这时候再滴加滴液都是过量的,结果当然偏大;而只滴到暗黄色则是未到终点,结果则是偏小。颜色变化的原因当然是指示剂甲基红造成的,因为甲基红的变色范围最大只达到pH6.2,溶液还属于弱酸性,也就是说溶液还有少量的H2SO4未参与反应,反过来讲NaOH标准液消耗量就偏小了。大家知道,强碱滴定强酸达到平衡时(也就是反应终点),其溶液的pH值应该是中性的(也就是pH=7.0)。所以正确的滴定终点颜色必须是亮黄色。综上所述,我们不难发现问题的关键就在于滴定终点的判断,说白点就是终点颜色的判断是否一致准确。 试样称量是否准确也是影响极差的关键要素。 读数是否准确一致也是重要的影响因素。 操作过程是否规范一致也会造成偏差。 由于浓硫酸是较强的干燥剂,吸湿能力很强,若装浓硫酸的胶帽滴瓶密封性不好,易引起硫酸吸收空气中的水分而造成硫酸试样浓度的不稳定不一致,从而影响测定结果。解决的办法是把硫酸试样稀释一倍,减小硫酸试样的吸湿性,保持硫酸试样浓度的稳定一致;同时,尽量快速称取试样,减小浓度波动;增加装试样的胶帽滴瓶的密封性,保证实验浓度的稳定一致。 通过以上的分析探讨,我们非常明确地知道硫酸含量平行测定结果极差偏大的各种原因,也非常清楚地知道影响极差的最为关键的因素。因此,在以后的实训教学中就能有的放矢地加以训练,提高同学们的滴定技能水平,进而成为合格的化学分析人员。 【参考文献】 (1)郭若鹭.分析化学.北京.中国轻工业出版社,1999.02 (2)王芳权.分析化学实验北京.中国轻工业出版社,1998.10
 爱华网
爱华网